- 2018-11-28
- 最新情報
- 3DPrinter, 3DPrinting, 3Dプリンター, 3Dプリンティング, FDM・FFF, filament, Materialise, Medical, Stratasys, Ultimaker, Ultimaker S5, テクノロジー, フィラメント, 医学, 医療
マテリアライズはFDA承認医療アプリケーションに対するUltimaker S5の互換性をテスト
オランダの3DプリンタメーカーUltimakerは、同社の最新FFF方式3Dプリンタ『Ultimaker S5』が、 ベルギーに本拠を置く3Dプリンティング・ソリューションと造形サービス企業マテリアライズ(Materialise)が提供するFDA(アメリカ食品医薬品局:Food and Drug Administration)承認の医療アプリケーション「Materialise Mimics inPrint」の認証を受けたことを発表した。

FDA(アメリカ食品医薬品局)のガイドラインでは、Materialise Mimics inPrintなどのFDA承認済みソフトウェアを使用し、Materialiseのソフトウェアと互換性のある3Dプリンタおよび材料をする使用し、診断およびその他の医療目的のための3Dモデルを作成することが定められている。
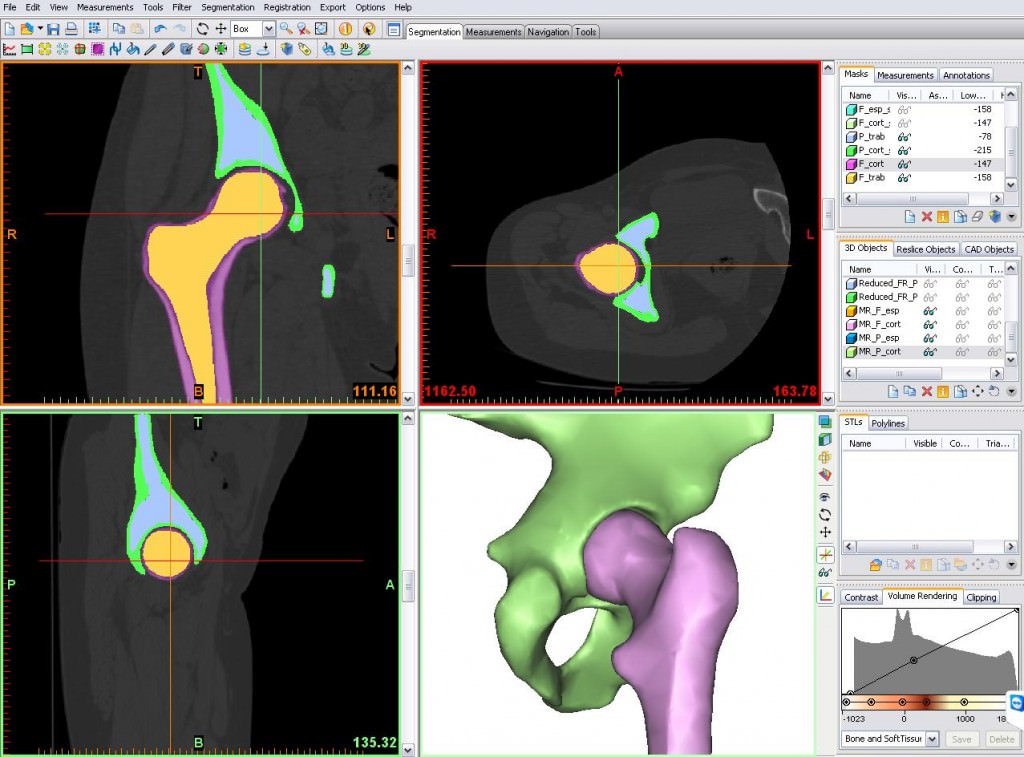
米国上位20病院のうち16病院がMaterialise Mimics inPrintソフトウェアを導入
マテリアライズは、Materialise Mimics inPrintソフトウェアを使用して、FDA承認の医療アプリケーションに対するUltimaker S5の互換性をテスト、部品品質の徹底的な分析を行った。
厳しい社内テストの結果、Ultimaker S5とMaterialise Mimics inPrintソフトウェアを組み合わせた3Dプリントワークフローが、医師や病院の安全性と品質管理の負担を軽減し、医療目的に適しているとして「Ultimaker S5」を認証した。

病院で使用可能なStratasys 3Dプリンタを検証
マテリアライズはこれまでに、術前検証など患者固有の解剖学的3Dモデル製作のため、Stratasysのハイエンド3Dプリンタ「J750」や「J735」などの一部機種とMaterialise Mimics inPrintソフトウェアを組み合わせた検証も行っている。
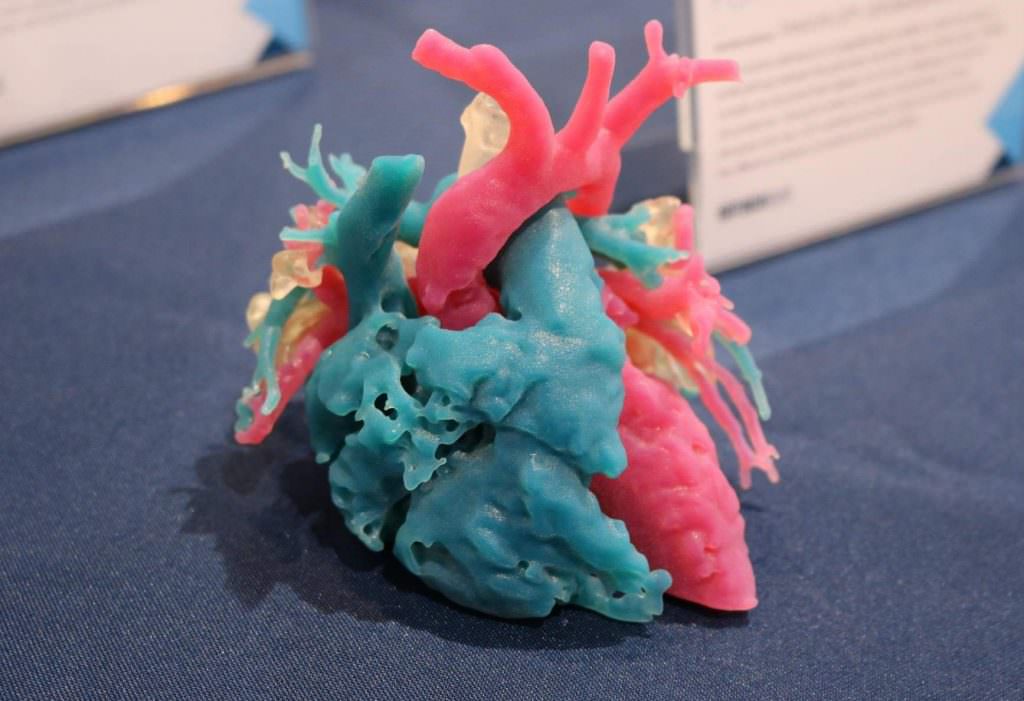
J750で3Dプリントされた心臓モデル
関連記事
- Ultimaker工業グレードの新型3Dプリンタ『Ultimaker S5』発表
- Ultimakerシンガポールに新オフィスを開設
- 超高解像度マイクロ部品用3Dプリンタ「Altraspin」
- 東京大学が高精度な頭部3DCGデータを無償公開
- 3Dプリントの世界的支出は2019年に138億ドルに達すると予測
- AutodeskとWHILLのコラボで実現したジェネレーティブデザイン
- 3Dプリント技術で乳癌治療法を追求する
- 放射線療法研究のため製作された3Dプリント製人体模型
- Canonが3Dプリンタ用セラミックス材料と作製技術開発
最新情報をお届けします
Twitter でid.artsをフォローしよう!
Follow @idarts_jp








